Produzione di dispositivi finiti all'avanguardia con la stampa in modalità controllata di Formlabs

I dispositivi per utilizzo finale devono mettere al primo posto la sicurezza del paziente. Man mano che le stampanti 3D sostituiscono gli strumenti tradizionali per la produzione di dispositivi medici, i fornitori di stampanti stanno facendo a gara per aggiudicarsi una fetta di mercato con approcci creativi e spesso non collaudati, come la stampa in modalità aperta. La stampa in modalità aperta consente ai clienti di usare qualsiasi materiale disponibile per la stampante senza particolari restrizioni. Questa modalità presenta senz'altro alcuni vantaggi nel breve termine, per quanto riguarda la selezione e la disponibilità del materiale, ma non tiene conto della sicurezza dei pazienti. I clienti e i pazienti confidano nel fatto che i fornitori del prodotto finito svolgano tutti gli accertamenti richiesti per garantire che i dispositivi siano precisi, affidabili e sicuri. Questo è possibile soltanto grazie a una rigorosa convalida dei flussi di lavoro, sottoposti a test e a controlli.
Inoltre, alla luce delle recenti modifiche dei requisiti normativi globali per la produzione di dispositivi medici, i workflow controllati sono in prima linea nell’implementazione di tecniche di produzione in grado di garantire il futuro dei produttori. All'inizio dell'anno scorso l'Australian Department of Health’s Therapeutic Goods Administration (TGA) , l'ente regolatore australiano per i prodotti terapeutici, ha annunciato un importante programma di riforma del regolamento per medicinali e dispositivi medici. Secondo i regolamenti in vigore, i produttori di dispositivi medici personalizzati sono esenti da requisiti normativi come ispezioni indipendenti e certificazione dei dispositivi medici personalizzati.1 Ma le modifiche introducono un nuovo concetto denominato Sistema di produzione dei dispositivi medici (SPDM) e un quadro di riferimento che regola i sistemi e prevede una revisione governativa della convalida completa. Se un cliente non utilizza un SPDM autorizzato, i suoi dispositivi medici richiederanno la stessa supervisione normativa cui sono sottoposti i dispositivi prodotti con metodi convenzionali. Per le cliniche e i laboratori indipendenti, questo significa che il produttore deve essere in grado di dimostrare di aver effettuato rigorosi test sulla sicurezza e sulle prestazioni prima dell'immissione sul mercato.1 Sarà dunque necessario certificare i materiali di consumo combinati con tutte le diverse attrezzature impiegate per la produzione del dispositivo per utilizzo finale.
Noi di Formlabs sappiamo che fornire accesso a soluzioni complete professionali e attente alla sicurezza per la produzione di dispositivi finali non è uno sprint, ma una maratona. Man mano che l'intero ecosistema di stampa si integra sempre di più con la produzione di dispositivi medici affidabili e sicuri, Formlabs si sta preparando a ottimizzare i tuoi flussi di lavoro con la stampa in modalità controllata secondo questi principi:
1. Gestione della qualità affidabile, dall’inizio alla fine
La modalità aperta può dare la soddisfazione a breve termine di avere un'applicazione immediatamente disponibile per la stampa. Purtroppo molti produttori non riescono a prevedere le potenziali criticità nel controllo della qualità. Ad esempio un produttore che offre la modalità aperta potrebbe rifiutare di assumersi la responsabilità se le resine di terze parti danneggiano la stampante o causano problemi, mentre i venditori di materiali non possono garantire la qualità delle prestazioni del dispositivo finale, dato che non controllano gli aggiornamenti e le modifiche alla stampante. Anche nel caso in cui sia i fornitori della resina che i produttori della stampante avessero strutture impeccabili con conformità ISO indipendenti, un produttore di stampanti in modalità aperta non è tenuto a monitorare le prestazioni della resina, e non è responsabilità dell'azienda produttrice della resina tenere traccia delle prestazioni della stampante. Di conseguenza, con la stampa in modalità aperta, non è possibile gestire in modo affidabile eventuali reclami post-commercializzazione o riferiti ad eventi avversi.
Essendo Formlabs un produttore di stampanti e resine, il suo sistema di gestione della qualità conforme alle norme ISO 13485 fornisce monitoraggio, manutenzione e controllo completo dell'intero workflow, dalla produzione del materiale nel nostro stabilimento in Ohio, Stati Uniti, fino alle interazioni tra materiali e attrezzature e ai test di prestazione e sicurezza dei dispositivi stampati prima dell'immissione sul mercato. La stampa in modalità controllata di Formlabs include inoltre procedure post-commercializzazione collaudate per la gestione dei reclami e per il monitoraggio degli eventi avversi tramite la nostra apposita unità di gestione dei reclami. Questi processi sono inoltre soggetti a controlli imparziali di routine da parte di terze parti e conformi ai requisiti normativi.
Le resine proprietarie biocompatibili di Formlabs, come la BioMed Clear Resin, vengono prodotte nella nostra struttura con certificazione ISO 13485 in Ohio, Stati Uniti.
2. Facilità di tracciamento
Poiché né il produttore della resina o né quello della stampante si assume la responsabilità dei problemi che si presentano con la stampa in modalità aperta, la risoluzione dei problemi relativi a stampanti in modalità aperta e resine di terze parti acquistabili indipendentemente può rivelarsi complicata. Inoltre, a meno che il produttore del dispositivo conservi ogni flacone dopo l'uso e riservi un serbatoio resina per ciascun flacone, è impossibile risalire all'hardware o allo specifico lotto di resina con cui si è verificata l'anomalia del dispositivo. Questo può generare confusione e aumentare le responsabilità ascrivibili al produttore, visto che non è chiaro chi debba gestire i reclami.
Con la stampa in modalità controllata di Formlabs basta una semplice telefonata al team del Dental Service Plan o del Medical Service Plan per associare facilmente il problema alle informazioni specifiche relative a PreForm, al firmware e al lotto di resina attraverso la Dashboard integrata per la risoluzione rapida dei problemi.
3. Convalida completa del workflow
In qualità di produttore di resine, Formlabs progetta i suoi materiali affinché siano adatti al workflow di stampa 3D stereolitografica di Formlabs, in modo da garantire prodotti affidabili con ogni stampa. Ogni materiale viene sottoposto a rigorosi test interni riguardanti la sicurezza e le prestazioni, così da garantire che soddisfi strettissimi requisiti specifici per hardware, software e prodotti finali, su un totale di più di 80 stampanti.2 Durante lo sviluppo dei materiali, le resine Formlabs sono testate da scienziati, medici ed esperti nei campi di ricerca e sviluppo, regolamentazione e discipline relative alla produzione. Questi esperti effettuano accurate valutazioni dei rischi sull'intero workflow, testando ogni passaggio, dalla produzione della resina al dispositivo biocompatibile finito sottoposto a polimerizzazione post-stampa. La valutazione dei rischi prende in considerazione gli eventuali pericoli, le soluzioni adottabili e l'efficacia delle soluzioni proposte per garantire la facilità d'uso delle resine Formlabs con tutta l'attrezzatura necessaria per la produzione di dispositivi medici biocompatibili. I workflow consigliati vengono testati esternamente dai leader del settore per assicurarsi che le resine siano adatte alle necessità del contesto clinico reale.
Poiché i dispositivi medici stampati in 3D sono relativamente nuovi sul mercato, i requisiti di sicurezza del settore applicati alla resina o ai produttori di stampanti non sono ben definiti. Il livello dei test di sicurezza effettuati dipende dall'azienda produttrice delle stampanti, dato che le impostazioni di stampa personalizzate di ciascuna stampante possono influire sulle prestazioni e sulla sicurezza del dispositivo ottenuto. Per capire l’approfondimento del processo di convalida al quale è stato sottoposto il dispositivo si possono consultare le raccomandazioni nelle istruzioni per l'uso.
Le prestazioni finali dell'oggetto stampato non sono definite finché il materiale non è sottoposto a post-elaborazione secondo le raccomandazioni nelle istruzioni per l'uso. Allo stato grezzo (cioè non ancora sottoposte a polimerizzazione post-stampa), le parti stampate sono malleabili e, se non vengono lavate o polimerizzate come indicato, possono portare a variazioni nelle prestazioni. Inoltre il tipo di stampante e di unità di lavaggio e di polimerizzazione post-stampa possono influenzare le prestazioni del dispositivo finito. Queste raccomandazioni sulla post-elaborazione potrebbero richiedere un'ottimizzazione a seconda delle specifiche impostazioni di stampa relative alla marca della stampante, nonché al tipo e alla marca delle attrezzature per la post-elaborazione. Se la post-elaborazione è ottimizzata dai produttori della stampante, questo risulterà evidente confrontando le istruzioni per l'uso del produttore di resina e della stampante.
La modalità di stampa controllata di Formlabs elimina le incertezze nella scelta della combinazione ottimale tra stampante e unità di post-elaborazione. Formlabs richiede l’ottimizzazione e lo svolgimento di test accurati dell'intero workflow per garantire la sicurezza dei pazienti in ogni fase. Questo è evidenziato nelle istruzioni per l'uso specifiche di ciascuno dei nostri prodotti, dove si possono trovare le migliori raccomandazioni per produrre dispositivi affidabili per un'ampia gamma di applicazioni. Per convalidare ulteriormente l'intero ecosistema di stampa, prima dell'immissione sul mercato tutta la documentazione rilevante e i risultati di stampa sono sottoposti a controlli e alla revisione da parte di organismi notificati ed enti regolatori sanitari (ad esempio l'Agenzia per gli alimenti e i medicinali degli Stati Uniti, FDA) per i requisiti normativi e di qualità non necessari per i workflow delle stampanti in modalità aperta. Inoltre, con la stampa in modalità controllata, tutti gli aggiornamenti di software per gli apparecchi sono testati accuratamente con tutta la gamma di materiali Formlabs, così da garantire ripetibilità e precisione degli oggetti prodotti da una stampante.
4. Presentazioni e approvazioni relative ai dispositivi medici
Come la maggior parte dei requisiti normativi globali, le linee guida dell'Agenzia per gli alimenti e i medicinali degli Stati Uniti (FDA) sul design e sulla produzione (sezione V) e sui test dei dispositivi (sezione VI) per i permessi relativi ai dispositivi medici 510(k) e le approvazioni prima dell'immissione sul mercato includono linee guida tecniche per soddisfare i requisiti di qualità del sistema, e riportano le informazioni essenziali specifiche per ciascuna candidatura, in modo che la presentazione della richiesta rispetti i tempi e abbia un esito positivo. Nel caso di dispositivi stampati in 3D, la stampa in modalità controllata di Formlabs fornisce ai produttori prove credibili che attestano la sicurezza e le prestazioni dei dispositivi, supportate dal Device Master File (MAF) archiviato dalla Agenzia per gli alimenti e i medicinali degli Stati Uniti (FDA). Nel Device Master File, Formlabs fornisce tutte le informazioni significative relative ai test sulle prestazioni, sulla sicurezza e sulle formulazioni proprietarie ai fini dell'esame da parte dell'Agenzia per gli alimenti e i medicinali degli Stati Uniti (FDA). I produttori possono richiedere l'identificazione del MAF di Formlabs per minimizzare i test necessari all'approvazione di dispositivi medici, con un conseguente risparmio di tempo e denaro. Questo è possibile solo grazie alla modalità controllata che garantisce la convalida del workflow dall'inizio alla fine.
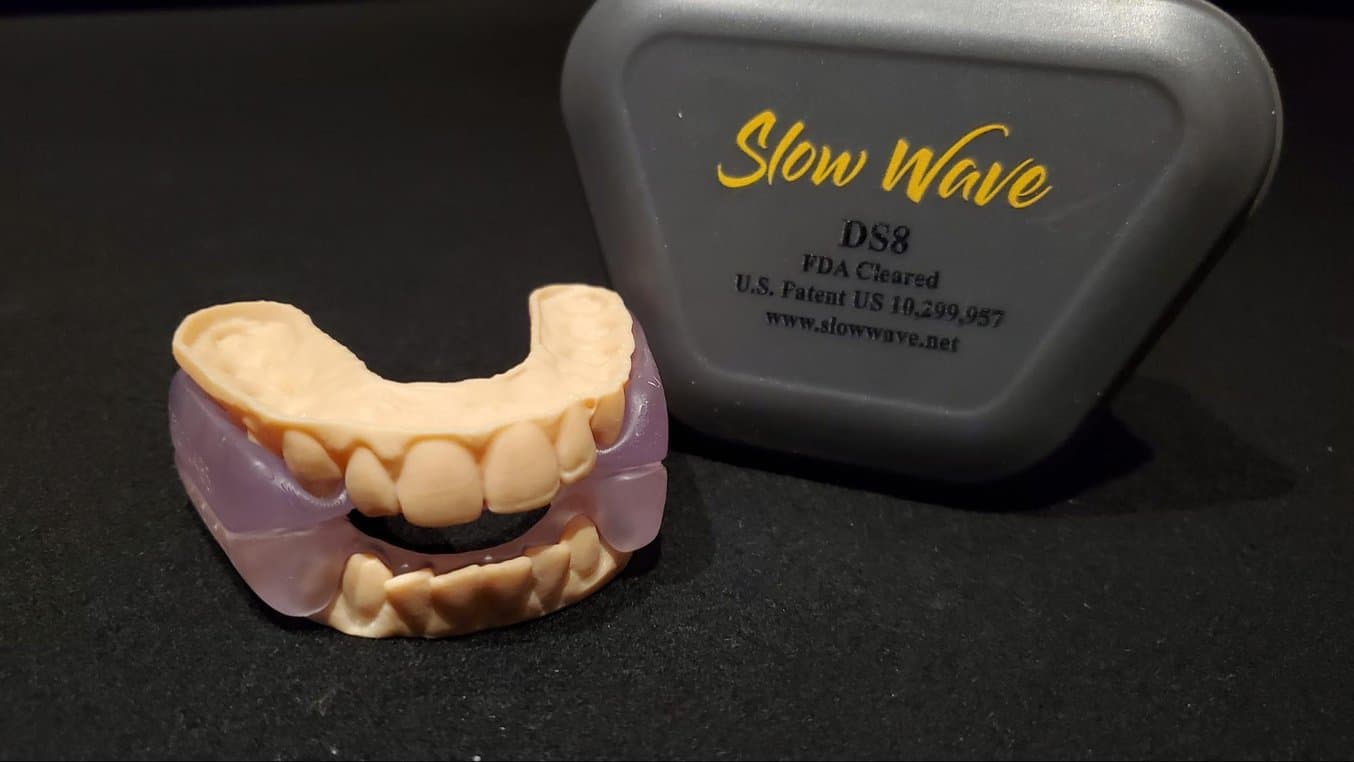
Il 2 ottobre 2020 il dispositivo Slow Wave DS8 è stato approvato secondo il modulo 510(K) dell'Agenzia per gli alimenti e i medicinali degli Stati Uniti (FDA), diventando la prima applicazione intraorale per il trattamento della roncopatia e delle apnee ostruttive nel sonno realizzata con la BioMed Clear Resin.
Al contrario, l'ambiguità della stampa in modalità aperta non consente strategie simili per la presentazione della richiesta di permessi. Con la stampa in modalità aperta, i produttori del dispositivo sono responsabili di tutti i test, infatti è quasi impossibile per l'azienda produttrice delle stampanti convalidare ciascun materiale con determinate impostazioni di stampa per un gran numero di combinazioni di unità di lavaggio e di polimerizzazione post-stampa. Inoltre i produttori di dispositivi per utilizzo finale potrebbero necessitare di informazioni specifiche per i materiali che non sono facilmente reperibili. Di conseguenza, una volta che un produttore è in grado di ottenere l'approvazione, il materiale e i workflow associati devono essere controllati per mantenere la qualità del dispositivo. Con molti attori in gioco, ad esempio il fornitore della resina, quello della stampante, e quelli dell'unità di lavaggio e di polimerizzazione post-stampa, assicurarsi che i materiali e i workflow approvati restino intatti può diventare insostenibile per il produttore del dispositivo.
La stampa in modalità controllata di Formlabs garantisce ai produttori la tranquillità di potersi concentrare sulla produzione di qualità di dispositivi sicuri dei quali i clienti si possano fidare.
5. Piattaforma per i partner nella realizzazione di materiali
Nel caso di materiali con brevetti privati inseriti sulla piattaforma per i partner nella realizzazione dei materiali Formlabs, come le resine per protesi dentali digitali, la Temporary CB Resin e la Permanent Crown Resin, il team di ricerca e sviluppo di Formlabs lavora a stretto contatto con i venditori di resina per convalidare le proprietà dei materiali e la sicurezza con impostazioni di stampa appositamente sviluppate per soddisfare le linee guida del settore per quanto riguarda stampabilità e prestazioni ottimali. Inoltre, gli identificativi del lotto di resina del venditore sono programmati in ciascuna cartuccia per mantenere la conformità di Formlabs con la certificazione ISO 13485. I materiali con brevetto privato sono anche collegati al Sistema di gestione della qualità e soggetti a controlli di terze parti per la documentazione relativa a potenziali eventi avversi al fine di garantire regolarmente l'affidabilità.
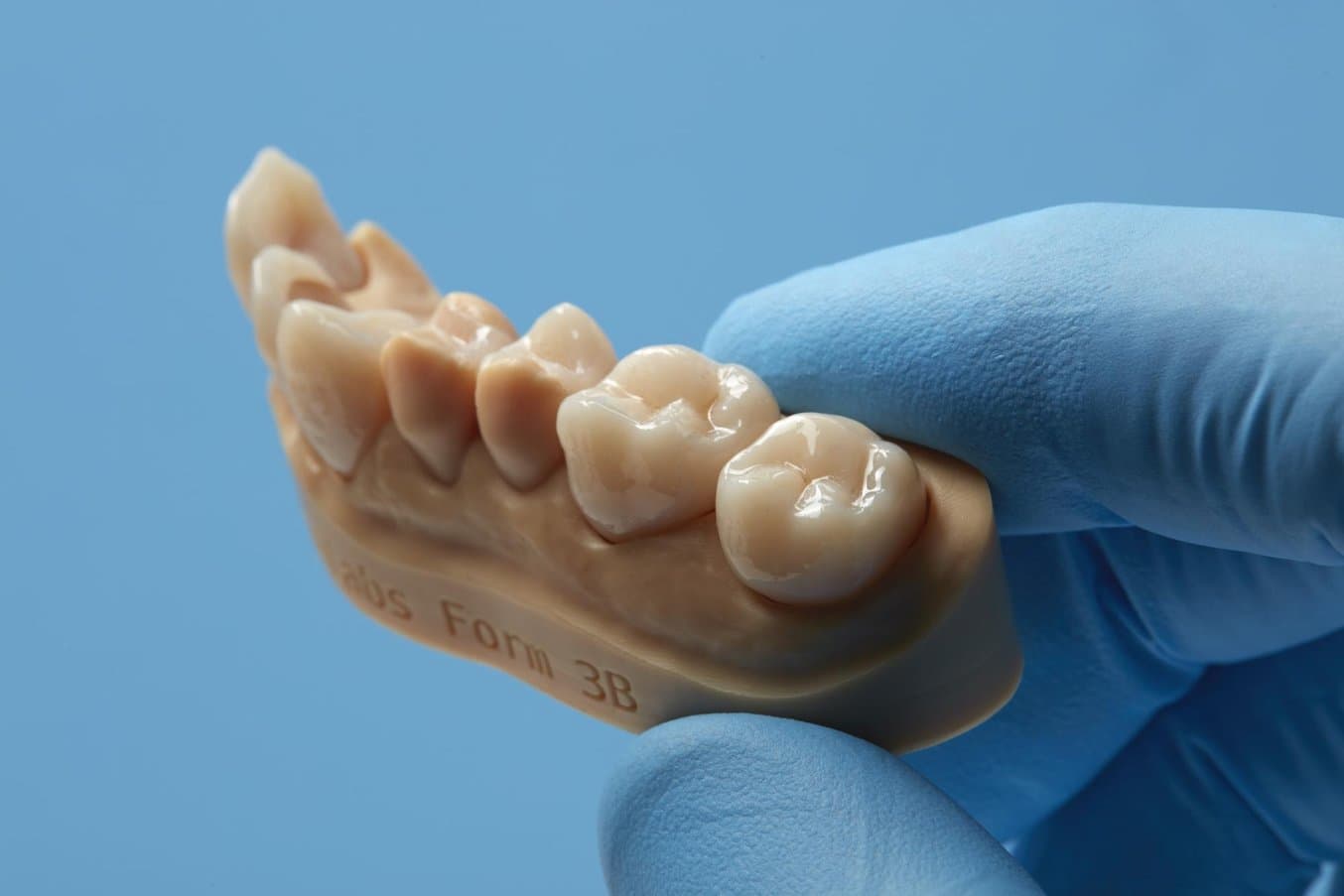
Nel caso di materiali con brevetti privati i come la Permanent Crown Resin, il team di ricerca e sviluppo di Formlabs lavora a stretto contatto con i fornitori della resina per convalidare le proprietà dei materiali e la sicurezza con le impostazioni di stampa.
Formlabs è inoltre responsabile delle importazioni regionali di alcuni materiali con brevetti privati. Questo vincola Formlabs a farsi carico della gestione dei reclami relativi ai requisiti e agli esami normativi, nonché dei protocolli di sicurezza già citati per mantenere un approccio globale all'esperienza degli utenti e rispettare le qualificazioni di sicurezza per tutti i materiali nell'ecosistema di Formlabs.
Conclusioni
Come nella guida di un veicolo, così nella scelta dei materiali per la stampa 3D, la velocità non coincide con la sicurezza. Man mano che le stampanti 3D diventano strumenti irrinunciabili per la produzione di dispositivi medici, gli enti regolatori globali stanno modificando le loro linee guida per gestire nuovi potenziali problemi di sicurezza. La modalità di stampa controllata di Formlabs consente di eliminare le incertezze e di avere la sicurezza che la resina e l'intero workflow siano stati convalidati per soddisfare le esigenze cliniche digitali di oggi.
1 Governo australiano, dipartimento della salute e dell'amministrazione di prodotti terapeutici. Dispositivi medici personalizzati (compresi dispositivi stampati in 3D) - Modifiche normative per dispositivi personalizzati, 23 dicembre 2020
2 la Permanent Crown Resin è compatibile solo con la Form 3B. Per avere questa sicurezza, la Permanent Crown Resin è stata convalidata con oltre 40 stampanti.