Abstrichtupfer für COVID-19-Tests aus dem 3D-Drucker
Was sind Abstrichtupfer?
Das Problem
Es gibt weltweit zu wenige Tupfer für Nasenrachenabstriche, mit denen COVID-19-Tests durchgeführt werden. Dieser Engpass wird sich vermutlich noch verschärfen, weil viele Regierungen und Gesundheitseinrichtungen die Anzahl der Tests signifikant steigern wollen, bevor Einschränkungen aufgehoben und normale Wirtschaftstätigkeiten wieder aufgenommen werden. Die aktuellen und zu erwartenden Engpässe in der Lieferkette sind dermaßen ernst, dass Mediziner bereits ihre eigenen Tupfer entwickeln und testen, welche so schnell und sicher wie möglich hergestellt werden müssen.
Diese Seite beschreibt entsprechende Bemühungen in Spanien. Lesen Sie mehr über die Entwicklung von Nasenrachentupfern in den USA.
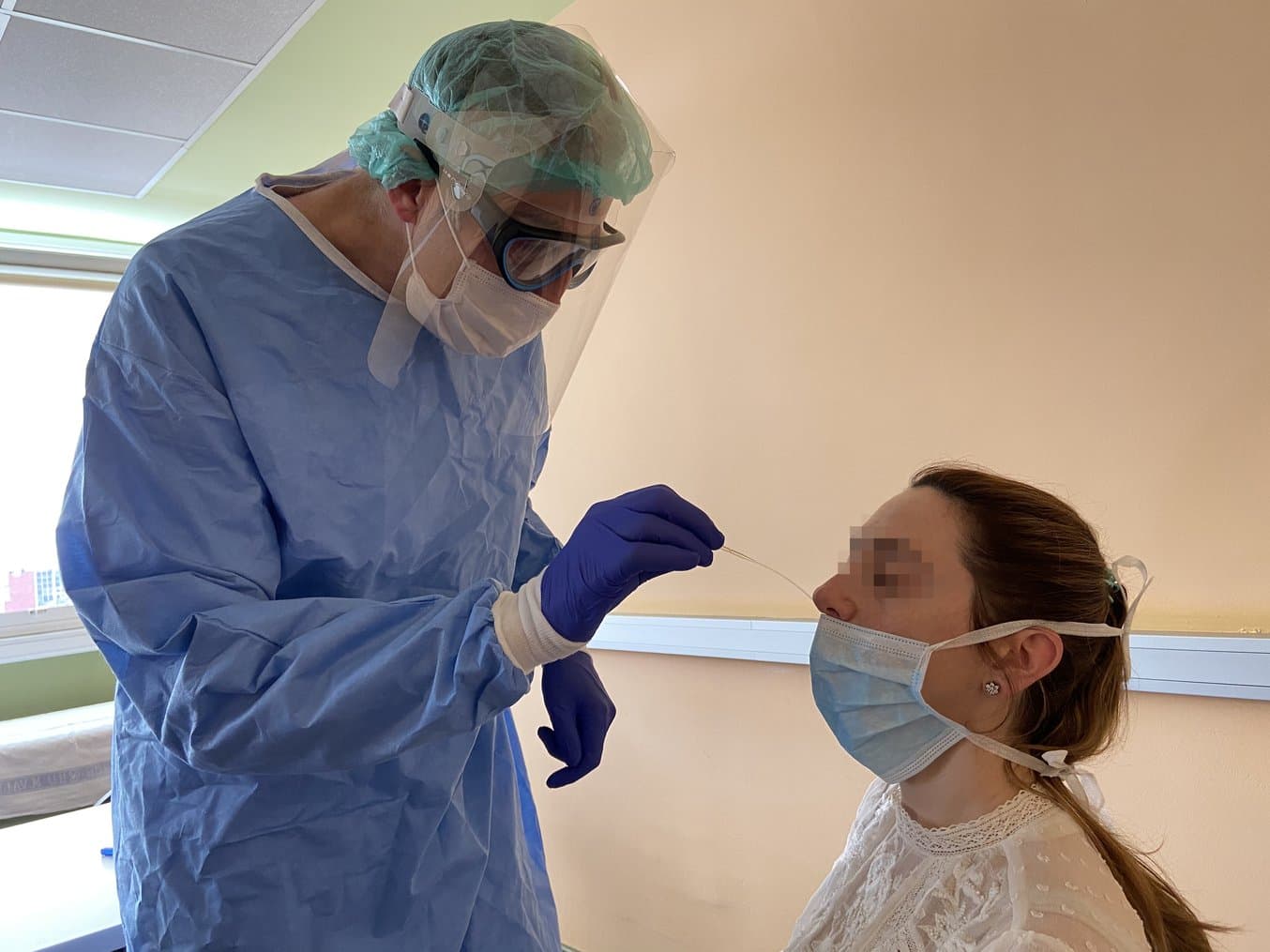
Nasenrachentupfer werden für gewöhnlich genutzt, um auf Grippe oder andere Atemwegserkrankungen zu testen. Es handelt sich um flexible Stäbchen mit Borsten am Ende, die in die Nase bis zur Nasenhöhlen-Rückwand eingeführt werden, um dort mit Wischbewegungen Material zu sammeln, das an den Borsten haften bleibt. Der Tupfer wird anschließend in ein mit einem Kulturmedium gefülltes Röhrchen gesteckt. Die Tupfer verfügen 7 bis 8 cm unterhalb der Borstenspitze über eine Sollbruchstelle, an der der Tupfer abgebrochen werden kann, damit er kurz genug ist, um das Röhrchen zu verschließen, bevor es zum Test ins Labor geschickt wird.
Wie werden Abstrichtupfer hergestellt?

Die Lösung
Das Hospital virtual Valdecilla (HvV) in Spanien
Als Mitarbeiter des Gesundheitssystems in der spanischen Region Kantabrien eine hohe Nachfrage und einen starken Lieferengpass bei Abstrichtupfern für COVID-19-Tests feststellten, kontaktierten sie das Hospital virtual Valdecilla (HvV) mit der Frage, ob diese Einrichtung in der Lage sei, Abstrichtupfer vor Ort in der Region zu entwickeln und herzustellen.
„Ich bin überzeugt: Womit wir heute hier konfrontiert sind, das erwartet in Kürze auch viele andere Regionen. Bevor wir die bestehenden Ausgangsbeschränkungen aufheben können, müssen wir mehr Personen testen. Daher brauchen wir mehr Abstrichtupfer. Aber das ist eine Herausforderung, weil auch die USA mehr Abstrichtupfer benötigen, und Italien und viele andere Länder und andere Regionen in Spanien“, erklärte Dr. med. Ignacio Del Moral, Geschäftsführer des Hospital virtual Valdecilla (HvV).
Das HvV setzte eine multidisziplinäre Forschungsgruppe aus Hals-Nasen-Ohren-Fachleuten (HNO), Mikrobiologen, Krankenpflegern und Ingenieuren ein, um mit den 3D-Druckern und biokompatiblen, autoklavierbaren Kunstharzen von Formlabs ein alternatives Design zu entwickeln und zu testen.Das Team entwickelte und testete alle zwei Tage neue Versionen, bis innerhalb von 10 Tagen ein endgültiges Design gefunden wurde – ein Prozess, der bei Medizinprodukten üblicherweise Monate dauert.
„Die letzte, fünfte Version wurde an über 100 Patienten getestet. Die HNO-Abteilung ist sehr zufrieden mit diesen Abstrichtupfern, weil sie hart, aber gleichzeitig auch sehr flexibel sind. Dadurch können wir Stellen tief in der Nasenhöhle zur Entnahme der biologischen Probe erreichen“, erklärte Juan Pedraja Vidal, Ingenieur für Medizinprodukte und Leiter des Labors für 3D-Druck und virtuelle Realität im HvV.
Unter Verwendung eines SLA 3D-Druckers von Formlabs kann das HvV innerhalb von 11 Stunden 324 Abstrichtupfer herstellen. Durch Drucken über Nacht werden so mit einem einzigen Drucker innerhalb von 24 Stunden 650 Abstrichtupfer produziert.
Die Schweizer Armee in der Schweiz

Als Folge der Knappheit von COVID-19-Testkits – insbesondere Nasenrachenabstrichtupfer – in der Schweiz sowie um die Abhängigkeit von internationalen Lieferketten zu mindern, initiierte der Oberfeldarzt der Schweizer Armee kollaborative Maßnahmen, die die Produktion ins Inland verlegen sollten. Der Oberfeldarzt ist in Sonder- und Ausnahmefällen für die Koordination der schweizerischen Gesundheitsressourcen sowie deren Vorbereitung und Einsatz verantwortlich.
Ein multidisziplinäres Expertenteam der GobiX GmbH entwarf dutzende Prototypen eines firmeneigenen Abstrichtupferdesigns. Bei einer Studie im April 2020 wurde das finale Tupferdesign erfolgreich an 440 Mitgliedern der Schweizer Armee getestet – unter Leitung eines Teams aus 10 Ärzten und medizinischen Laboranalysten.
Prof. Patricia Schlagenhauf, Co-Direktorin des WHO Collaborating Centre for Travellers’ Health an der Universität Zürich (UZH) und COVID-19-Forschungskollegin von Michel Bielecki, Mitbegründer von GobiX, merkte an: „Der Zugang zu Tests und Testkits ist äußerst wichtig, insbesondere in gefährdeten Ländern mit begrenzten Ressourcen. Selbst in den Industrieländern waren die Testkapazitäten suboptimal, besonders zu Beginn der Pandemie. Das lag hauptsächlich an einem Mangel der Testmaterialien und Probeentnahmeflüssigkeiten. Umfassende Tests sind wirklich die beste Möglichkeit, die Entwicklung der Pandemie zu überwachen. Die Devise der WHO zur Kontrolle von COVID-19 ist einfach und effektiv. Sie lautet: ‚TESTEN, TESTEN, TESTEN‘. Ohne Tests können Entwicklungsländer niemals die Ausbreitung von COVID-19 überwachen und in den Griff bekommen.“
Validierungsstatus
Das Hospital virtual Valdecilla (HvV) in Spanien
Die mittels 3D-Druck hergestellten Abstrichtupfer wurden an mehr als 100 Patienten in Spanien getestet, um sie auf Patientensicherheit und Gebrauchstauglichkeit zu prüfen und um sicherzustellen, dass sie wie vorgesehen funktionieren und den Patienten nicht schaden. Das HvV hat auch ein Fertigungsverfahren festgelegt – vom 3D-Druck über die Reinigung, Nachhärtung und Qualitätskontrolle – bei dem sterilisierte Werkzeuge eine aseptische, kontrollierte Umgebung garantieren.
Die interne klinische Prüfung wurde von Medizinern der Mikrobiologie- und HNO-Abteilungen am Universitätskrankenhaus Valdecilla durchgeführt. Nach der internen klinischen Prüfung wurden die 3D-gedruckten Abstrichtupfer von den Gesundheitsbehörden der spanischen Region Kantabrien für den klinischen Einsatz zugelassen.
Das HvV stellt nun Abstrichtupfer her und stellt sie Medizinern in der Region und in Krankenhäusern anderer Regionen des Landes zur Verfügung. Ein zweiter 3D-Drucker ist unterwegs. So kann man dann ausreichend Abstrichtupfer herstellen, um als eine der ersten Regionen in Europa bei der Produktion dieses wesentlichen Teils der PCR-Tests autonom zu werden.
Das HvV führte in Zusammenarbeit mit dem regionalen Technologieinstitut Centro tecnológico CTC auch mechanische Tests durch, um das Verhalten der Abstrichtupfer unter Belastung zu prüfen und Daten zu sammeln, bei welcher Biegung des Teils es zum Bruch kommt. Hier finden Sie die Ergebnisse der mechanischen Prüfung (auf Spanisch).
Die Forscher möchten nun weitere Daten sammeln, um die Wirksamkeit der 3D-gedruckten Abstrichtupfer mit der herkömmlicher Tupfer zu vergleichen und die Ergebnisse in einer wissenschaftlichen Zeitschrift zu veröffentlichen. Das HvV arbeitet auch mit anderen Organisationen aus dem Gesundheitswesen zusammen, um Informationen über die Abstrichtupfer zur Erlangung des CE-Kennzeichens zu sammeln und einzureichen. Das Kennzeichen bescheinigt, dass das Medizinprodukt bestimmte „wesentliche Anforderungen“ der EU-Richtlinie über Medizinprodukte erfüllt (d. h. dass es sicher und für den vorgesehenen Zweck geeignet ist).
Die Schweizer Armee in der Schweiz

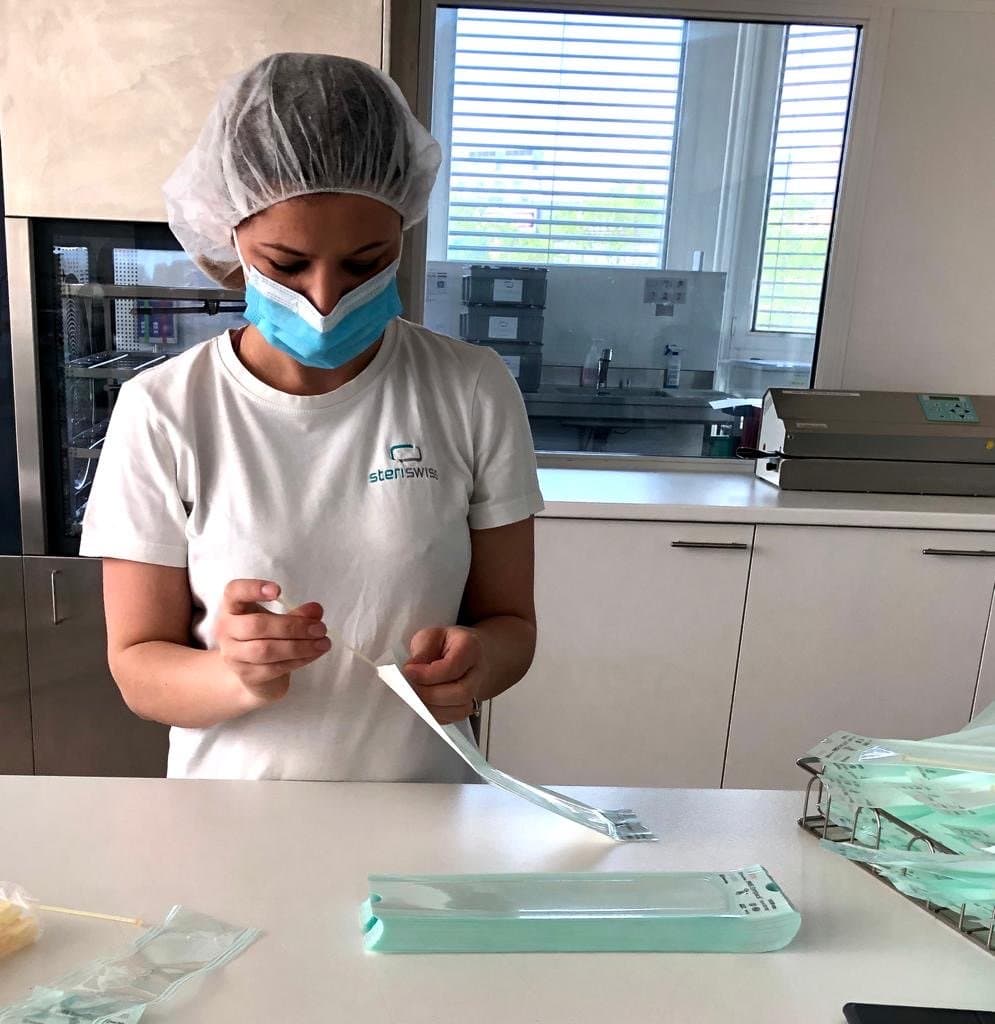
Die Abstrichtupfer wurden von einem Team aus 10 Ärzten und medizinischen Laboranalysten auf Probeentnahmeeffizienz, Testleichtigkeit und Patientenkomfort überprüft, als der erste COVID-19-Ausbruch im schweizerischen Ticino auftrat. 440 Mitglieder der Schweizer Armee nahmen an diesem Test teil.
Die Abstrichtupfer sind als Medizinprodukt der Klasse I CE-zertifiziert und befinden sich in Produktion. Die GobiX GmbH stellt die Abstrichtupfer her und verpackt sie für die Auslieferung an Testgebiete im gesamten Land.
Abstrichtupfer herstellen
Das Hospital virtual Valdecilla hat den Entwurf der Abstrichtupfer im Open-Source-Format öffentlich zur Verfügung gestellt, sodass andere Einrichtungen, die mit Engpässen konfrontiert sind, selbst Abstrichtupfer herstellen können.
Bitte beachten Sie, dass es im Verantwortungsbereich des Krankenhauses bzw. der Einrichtung liegt, den Arbeitsablauf zu prüfen, Desinfektionsverfahren anzuwenden, die Qualität der Abstrichtupfer zu bestätigen und den lokalen Genehmigungen und Freigaben zu entsprechen.
Für die Herstellung der Abstrichtupfer ist ein SLA 3D-Drucker des Typs Form 2 oder Form 3B erforderlich sowie das autoklavierbare, biokompatible Kunstharz Surgical Guide Resin.
Wenn Sie an der Herstellung von Abstrichtupfern oder am Kauf von Formlabs' 3D-Druckern und Materialien für den medizinischen Einsatz interessiert sind, kontaktieren Sie uns bitte direkt.
In Zusammenarbeit mit
Formlabs möchte unserem Partner Domotek für seinen Beitrag zu diesem Projekt danken.
Haftungsausschluss
Formlabs hat diese Website eingerichtet und ist im Rahmen der weltweiten Gesundheitskrise in unterschiedlichem Umfang in den hier beschriebenen Projekten involviert. Formlabs arbeitet an vielen Projekten, um auf die weltweiten Engpässe im Gesundheitswesen zu reagieren, doch auch bei der Behebung dieser Engpässe steht die Patientensicherheit für Formlabs weiter im Vordergrund. Wir müssen alle Personen, die an Lösungen dieser Engpässe arbeiten, darauf hinweisen, dass Masken, Abstrichtupfer, Schutzvisiere und andere 3D-gedruckte Produkte zum Schutz vor oder zur Behandlung von COVID-19 Medizinprodukte sind, die für die bestimmungsgemäße Verwendung sicher sein müssen. Wer diese Produkte herstellen möchte, sollte Folgendes beachten:
-
Formlabs ist ein Hersteller von 3D-Druckmaterialien, mit denen fertige Medizinprodukte in Übereinstimmung mit dem ausgewiesenen Verwendungsbereich hergestellt werden können. Und jedes andere Produkt, das mit diesen Materialien hergestellt wird, muss für den jeweiligen Verwendungszweck verifiziert und validiert werden.
-
Möglicherweise stellen Sie ein Produkt her, das nicht über die behördliche Zulassung und Freigabe verfügt. Wenn Sie Produkte herstellen, befolgen Sie die Richtlinien auf dem Etikett des jeweiligen Materials. Es ist ratsam, zuverlässigen regulatorischen Rat einzuholen.
-
Berücksichtigen Sie örtliche Vorschriften, Materialsicherheitsdatenblätter, Softwarefunktionen sowie Sterilisations- und institutionelle Anforderungen, bevor Sie Medizinprodukte drucken.
-
Regulierungsbehörden (wie das BfArM oder das britische MHRA) können eventuell die Überprüfung von Herstellungsinformationen und/oder Vorvermarktungsgenehmigungen beschleunigen.
Formlabs übernimmt keine Garantie, dass Produkte, die nicht von Formlabs selbst hergestellt wurden, ihrem Verwendungszweck entsprechen. Formlabs hat die in dieser Fallstudie genannten Designteile und deren Sicherheit bzw. Tauglichkeit für die beabsichtigte Verwendung weder unabhängig geprüft noch validiert. Alle 3D-gedruckten Vorrichtungen, die einem Hautkontakt ausgesetzt sind, sollten die Biokompatibilitätsanforderungen nach ISO 10993-1 erfüllen.